反応
ハロゲン化アルキルの有用な特性は、他の種類の化合物に容易に変換できることです。ハロゲン化アルキルの3つの最も重要な反応は、求核置換、脱離、および有機マグネシウム化合物への変換です。
求核置換
次の一般式で表すことができる求核置換により、ハロゲンを酸素、硫黄、窒素、または別の炭素で置き換えることができます。
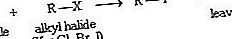
負に帯電した求核剤Yのソースは、-通常、イオン性ナトリウム又はカリウム塩(NAの+ Y -またはK + Y - )。求核置換の具体例は、水酸化ナトリウムと塩化ベンジルの反応です。

ハロゲン化アルキルの反応性の相対的な順序は、炭素とハロゲンの結合強度によって決まります。ヨウ化アルキルは最も弱い炭素-ハロゲン結合を持ち、最も速い速度で反応します。フッ化アルキルは最も強い炭素-ハロゲン結合を持ち、非常にゆっくりと反応するため、求核置換を受けることはほとんどありません。
有機化合物のさまざまなファミリーは、求核試薬の適切な選択によって調製できます。これらには、エーテル(ROR ')、エステル(RCOOR')、ニトリル(RCN)、および硫化物(RSR ')が含まれます。

フッ化アルキルは通常、塩化アルキル、臭化物、またはヨウ化物に対する求核剤として作用するフッ化物(例:NaF + RX→RF + NaX)によって調製されます。反応は原則として可逆的ですが、炭素-フッ素結合の強度が大きいほど、フッ化アルキルは塩化アルキル、臭化アルキル、またはヨウ化アルキルよりも優勢になります。ヨウ化アルキルは、ヨウ化ナトリウム(NaI)のアセトン溶液(CH 3 COCH 3)と反応させることにより、塩化アルキルと臭化アルキルから調製できます。この場合、塩化ナトリウム(NaCl)も臭化ナトリウム(NaBr)もアセトンに溶解しないため、反応は表示された方向に進みます。反応混合物から塩化ナトリウムまたは臭化ナトリウムが沈殿すると、平衡の位置が右に移動します。

化学者は一般に、ここまでに説明したハロゲン化アルキルの反応は、求核剤が結合の反対側から脱離基へとハロゲン化アルキルに近づくというメカニズムを通じて起こることに同意します。置換は、攻撃される炭素が求核試薬と脱離基の両方に部分的に結合している遷移状態(高エネルギー、不安定、非分離構造)を介して単一のステップで発生します。2つの種を含む任意のワンステッププロセスは二分子として定義され、この反応メカニズムはS N 2(置換求核二分子)と呼ばれます。

二分子求核置換の割合は、ハロゲン化アルキルの構造に強く依存し、求核攻撃を受けている炭素での混雑の程度によって支配されると考えられています。ハロゲン化メチル(CH 3 X)は最も速い速度で反応します。ハロゲン化第一級アルキル(RCH 2 X)はハロゲン化第二級アルキル(RR'CHX)よりも速く反応し、次にハロゲン化第三級アルキル(RR'R''CX)よりも速く反応します。置換基R、R '、およびR' 'が小さい場合(例:CH 3 XのR = R' = R '' = H)、遷移状態はあまり混雑せず、求核試薬は脱離基を炭素から急速に置換します。R、R '、およびR' 'をアルキル基で連続的に置換すると、求核剤の炭素へのアプローチがますます妨げられ、遷移状態がより混雑し、速度が遅くなります。近くのグループによる反応部位へのアクセスの遮断は、立体障害と呼ばれます。
三級ハロゲン化アルキルは非常に立体的に妨げられているため、求核置換を受けると、S N 2 以外のメカニズムでそうなります。2段階のメカニズムが続くと考えられています。最初のステップは2番目のステップよりも遅く、反応の全体的な速度。

律速(遅い)ステップには1つの分子しか含まれないため、メカニズムは単分子として記述され、S N 1(置換求核性単分子)という用語が適用されます。遅いステップで形成される種は、正に帯電した電子不足の炭素を含み、カルボカチオンと呼ばれます。カルボカチオンは不安定であり、求核剤などの結合形成に利用可能な非共有電子を持つ物質と急速に反応します。
除去
攻撃種が水酸化物などの強塩基である場合(- OH)又はアルコキシド(- OR)、求核置換反応は、合成の目的は、ハロゲン化アルキルがプライマリである場合にのみ実用的であるために行います。強塩基が第二級または第三級ハロゲン化アルキルと反応するときに観察される主な反応は、2-クロロ-2-メチルプロパンに対するナトリウムメトキシドの攻撃の場合のように、脱離です。

置換を有する除去競合するには、負に荷電したイオン、この場合はメトキシであるため(- OCH 3)、のいずれか(求核試薬として作用)炭素を攻撃することができ、または(塩基として作用する)プロトンを除去します。除去に伴う結合の変化は、電子対の動きを追跡するために曲線矢印表記を使用して表されることがよくあります。

説明されている方法でのハロゲン化アルキルの脱離は、単一のステップで発生すると考えられ、脱離二分子を表す機構記号E2が与えられます。除去は常に求核置換を伴い、求核置換の効率的な合成アプリケーションに対する主な制限です。十分に強い塩基を使用することで、通常、脱離を置換よりも優先させることが可能であり、E2メカニズムによるハロゲン化アルキルの脱ハロゲン化水素は、アルケンを調製する主な方法の1つです(炭化水素を参照)。






![アメリカの絶滅危惧種法[1973] アメリカの絶滅危惧種法[1973]](https://images.thetopknowledge.com/img/politics-law-government/2/endangered-species-act-united-states-1973.jpg)