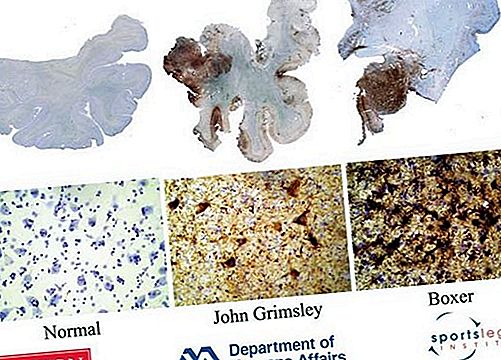
胸水
上記のシステムをガス圧力の計算で検討しますが、コンテナ壁の領域Aを小さな穴に置き換えます。時間tで穴から脱出する分子の数は、(1/2)(N / V)v z(At)に等しくなります。この場合、分子間の衝突が顕著であり、結果は非常に薄い壁の小さな穴にのみ(平均自由行程と比較して)保持されるため、穴の近くに近づく分子は、別の分子と衝突することなく通過し、そらされている。Vの関係Zと平均速度vはかなり簡単である:V Z =(1/2)V。
同じ穴から流出する2つの異なるガスの速度を比較すると、毎回同じガス密度から開始すると、重いガスよりもはるかに軽いガスが漏れ、低温よりも高温で多くのガスが漏れることがわかります。 、他の条件は同じです。特に、
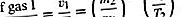
最後のステップは、エネルギー式(1/2)mv 2 =(3/2)kTに従います。ここで、(v 2)1/2は、v 2と(v̄)2が実際に異なる場合でも、vに近似されます単一に近い数値要素(つまり、3π/ 8)。この結果は、一定の温度の場合にグラハムが1846年に実験的に発見したものであり、グラハムの流出の法則として知られています。分子量の測定、蒸気圧の低い材料の蒸気圧の測定、または液体または固体表面からの分子の蒸発率の計算に使用できます。
熱蒸散
同じガスで温度が異なる2つの容器が小さな穴で接続されていて、ガスが定常状態になっているとします。穴が十分に小さく、ガス密度が低いために噴出のみが発生する場合、平衡圧力は高温側で高くなります。しかし、両側の初期圧力が等しい場合、ガスは低温側から高温側に流れ、高温圧力が上昇します。後者の状況は熱蒸散と呼ばれ、定常状態の結果は熱分子圧力差と呼ばれます。これらの結果は、理想的なガスの法則を使用してN / Vをp / Tに置き換えた場合、単純に流出式から得られます。
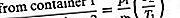
定常状態に到達すると、流出率は等しくなるため、
この現象は1879年にオズボーンレイノルズによって実験的に調査されました。細管を介して室温で圧力計に接続することにより、極低温または極高温で容器内のガス圧を測定すると、エラーが発生する可能性があります。ガスの連続循環は、2つのコンテナを、平均自由行程と比較して直径が大きい別のチューブに接続することによって生成できます。圧力差により、粘性のある流れによってガスがこのチューブを通過します。この循環流に基づく熱機関は、残念ながら効率が低い。






![アメリカの絶滅危惧種法[1973] アメリカの絶滅危惧種法[1973]](https://images.thetopknowledge.com/img/politics-law-government/2/endangered-species-act-united-states-1973.jpg)