多価硫黄の有機化合物:スルホキシドとスルホン
有機酸素化合物に相当するものがない有機硫黄化合物の2つの主要なグループは、スルホキシドとスルホンです。これらの化合物の結合が二重結合構造(スルホキシドの場合は「S(= O)」、スルホンの場合は「S(= O)2」)で表される場合、硫黄原子はそれぞれ10と12の価電子を「見る」。これはオクテットルールが許可する以上のものですが、硫黄は結合に3d軌道を利用できるため、オクテットルールに拘束されません。六フッ化硫黄(SF 6)。硫黄原子価殻が8個を超える電子に対応するように拡張する理論的なサポートはありますが、3d軌道は硫黄3sおよび3p軌道よりもエネルギーがはるかに高いため、結合スキームでの3d軌道の使用は批判されています。代替結合モデルは、-S等の極性結合呼び出し+(-O -のためのスルホキシドおよび-S - )2+(-O - )2-スルホンため。極共鳴構造が全体的な結合に寄与していることは明らかですが、硫黄3d軌道からもある程度寄与している可能性があります。スルホキシド基には硫黄原子上に孤立電子対も含まれるため、スルホキシド基はアミンと同様に非平面である必要がありますが、カルボニル基の平面構造とはかなり異なります-C(= O )―、スルホキシド基と比較されることもある。スルホキシドグループの非平面性の重要な結果は、RとR 'が異なるタイプR(S = O)R'のスルホキシドはキラルであり、実際には光学活性型でスルホングループを使用して分離できることです。四面体です。アミンとは対照的にホスフィンに似ていますが、三配位硫黄(3つの配位子と硫黄上の孤立電子対を持つ三角ピラミッド型硫黄化合物—たとえば、塩化スルフィニル、亜硫酸エステル、スルホキシド、チオスルフィン酸塩、およびスルフィリミンに見られます)硫黄への結合が長い(混雑が少ない)と、孤立したペアのs特性(ハイブリダイゼーションで使用される軌道の総数に占める軌道のパーセンテージ)が多いため、安定した構成。多くの光学活性三配位化合物が自然界に存在し、光学活性硫黄化合物は他のキラル化合物の合成に広く使用されています。
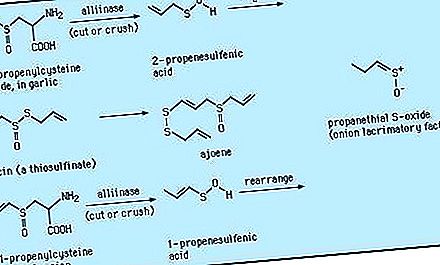
スルホキシドは、「S(= O)」グループに接続された2つの有機基をアルファベット順に指定し、その後にスルホキシドという単語を続けて指定します(例:エチルメチルスルホキシド、CH 3 S(O)C 2 H 5) 、または粒子-sulfinyl-(例、4-(メチルスルフィニル)安息香酸)を使用して、より単純なグループの名前から接頭辞を形成する。スルホンの命名法はスルホキシドの命名法に似ています。粒子-スルホニル-は複雑な場合に使用されます。ほとんどのスルホキシドは、融点の低い無色の液体または固体です。低分子量のスルホキシドジメチルスルホキシド(CH 3 S(= O)CH 3、DMSO)は水溶性で、毒性が低く、優れた溶媒です。それは急速に皮膚に浸透する異常な能力を有し、このようにして皮膚を通して化合物を運ぶことができます。それは獣医学、特に馬の跛行の治療にいくつかの用途があります。スルホンは通常無色の結晶性固体です。ジメチルスルホンは水溶性です。ジアリールスルホン(pH 2 NC 6 H 4 SO 2 C 6 H 4 NH 2 -p;例えばダプソン)および関連化合物は、結核およびハンセン病の治療に使用されてきた。「SO 2 C 6 H 4」ユニットをポリマー内に組み込んだポリスルホン樹脂は、電気部品や自動車部品など、優れた熱安定性と耐酸化性を必要とするアプリケーションに大規模に使用されています。
発生と準備
自然源から単離された化合物の中で、S-アルキルシステインS-オキシド(S-1-およびS-2-プロペニルシステインS-オキシドなど)(アリウム属の植物の風味料の前駆体)が最初に発見されました。炭素および他の元素(硫黄)での光学活性。腫瘍の成長を阻害すると報告されているブロッコリーのスルフォラファン(CH 3 S(O)(CH 2)4 NCS)やタマネギの抽出物からのzwiebelanes など、他のさまざまなスルホキシドが天然源から分離されています。DMSOは100万分の3(ppm)以下のレベルで広く見られ、海水を含む天然水の一般的な成分です。DMSOは、ジメチルスルホンとともに、藻類の代謝を通じて生成される場合があります。DMSOは、雨水で検出された場合、大気中の硫化ジメチル(CH 3)2 Sの酸化に起因する可能性があります。これは、地球規模の硫黄サイクルにおける生物起源の硫黄の自然移動の一部として発生します。
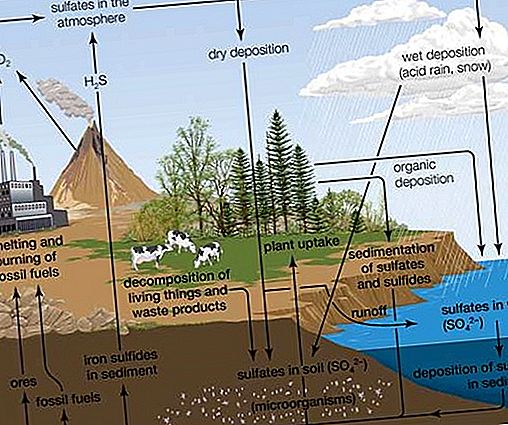
スルホキシドは、メタ過ヨウ素酸ナトリウム(NaIO 4)または過酸化水素(H 2 O 2)などの試薬で硫化物を酸化することにより簡単に調製できます。商業的には、DMSOは空気/一酸化窒素を触媒とする硫化ジメチルの酸化から作られますが、これは紙の製造のためのクラフト硫酸塩プロセスの主要な副産物です。たとえば過マンガン酸カリウムKMnO 4を使用する場合のように、硫化物またはスルホキシドのより強力な酸化により、スルホンが生成されます。光学活性なスルホキシドは、光学活性な酸化剤または微生物学的酸化剤でR R R 'であるタイプRSR'の硫化物を酸化することによって調製できます。あるいは、光学活性スルホキシドは、光学活性スルフィニル誘導体RS(= O)X(X = O、N、またはS)とR'LiまたはR'MgBrなどの試薬との反応を介して調製することができる。溶媒スルホラン(チオランS、S-ジオキシド)は、最初に二酸化硫黄をブタジエンと反応させてスルホレン(環状の不飽和5員環スルホン)を生成し、次に水素化してスルホランを生成することによって調製されます。

芳香族スルホンはまた、塩化スルホニルと芳香族炭化水素との反応により製造することができる。チオフェンの酸化によって形成されるチオフェンS-オキシドおよびS、S-ジオキシドは、硫黄上の電子の1つまたは両方のペアを酸素で置き換えることにより芳香族性が失われるため、親チオフェンよりもはるかに反応性が高くなります。