トリウム(Th)、周期表のアクチノイド系列の放射性化学元素、原子番号90; それは有用な原子炉燃料です。トリウムはスウェーデンの化学者であるJönsJacob Berzeliusによって発見されました(1828年)。銀色の白ですが、空気に触れると灰色または黒になります。それは、鉛の約半分の量であり、地球の地殻のウランより3倍豊富です。トリウムは鉱物のモナザイトから商業的に回収され、トライトやトリアナイトなどの他の鉱物にも発生します。金属トリウムは、四フッ化物(ThF 4)と二酸化物(ThO 2)の還元、および四塩化物(ThCl 4)の電気分解により、商業的に生産されています。この要素は北欧の神トールにちなんで名付けられました。
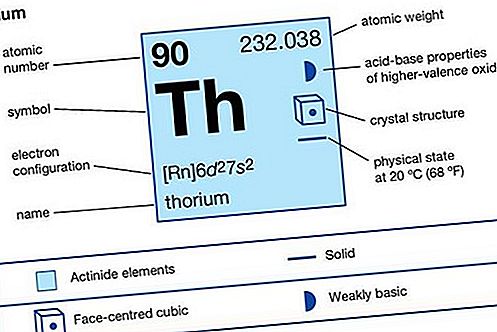

アクチノイド要素:アクチノイドの実用化
トリウムはまた、その同位体の1つであるトリウム232を
。
金属は、押し出し、圧延、鍛造、スエージ加工、および回転することができますが、トリウムの引張強度が低いため、伸線は困難です。これと、融点や沸点などのその他の物理的特性は、炭素や二酸化トリウムなどの特定の不純物の少量によって大きく影響されます。マグネシウムおよびマグネシウム合金にトリウムを添加して、高温強度を向上させます。これは、2000〜3750オングストロームの範囲の波長の紫外光を測定するために、市販の光電セルで使用されています。ガラスに加えて、トリウムは、特殊な光学用途に役立つ高屈折率のガラスを生み出します。以前はガスおよび灯油ランプのマントルのコンポーネントとして大きな需要があり、電球および真空管用のタングステンフィラメントの製造に使用されています。
トリウムの放射能は、ドイツの化学者ゲルハルトカールシュミットとフランスの物理学者マリーキュリーによって独立して発見されました(1898年)。自然トリウムは放射性同位元素の混合物であり、主にトリウム放射性崩壊シリーズの親である非常に長寿命のトリウム232(1.40×10 10年半減期)です。他の同位体は、ウランとアクチニウムの崩壊系列で自然に発生し、トリウムはすべてのウラン鉱石に存在します。トリウム232は、低速で移動する中性子を捕獲すると核分裂してウラン233に崩壊するため、増殖炉で有用です。合成同位体が準備されました。合成アクチノイド元素ネプツニウムに由来する崩壊鎖で形成されたトリウム229(7,880年の半減期)は、通常のトリウム(トリウム232)のトレーサーとして機能します。
トリウムは、ほとんどすべての化合物で+4の酸化状態を示します。Th 4+イオンは多くの複雑なイオンを形成します。二酸化チタン(ThO 2)は非常に難溶性の物質であり、多くの工業用途があります。硝酸トリウムは市販の塩として入手可能です。
要素のプロパティ
| 原子番号 | 90 |
|---|---|
| 原子量 | 232.038 |
| 融点 | 約1,700°C(3,100°F) |
| 沸点 | 約4,000°C(7,200°F) |
| 比重 | 約11.66(17°C) |
| 酸化状態 | +4 |
| 気体の原子状態の電子配置 | [Rn] 6d 2 7s 2 |









![ケベック州法イギリス[1774] ケベック州法イギリス[1774]](https://images.thetopknowledge.com/img/politics-law-government/5/quebec-act-great-britain-1774.jpg)


