弾性特性
希土類金属の他のほとんどの特性と同様に、希土類金属の弾性率は他の金属元素の中央のパーセンタイルに分類されます。スカンジウムとイットリウムの値は、ランタニドの端のメンバーの値とほぼ同じです(エルビウムからルテチウム)。原子番号の増加に伴い、弾性率が一般的に増加します。セリウム(一部の4f結合)とイッテルビウム(二価性)の異常値は明らかです。
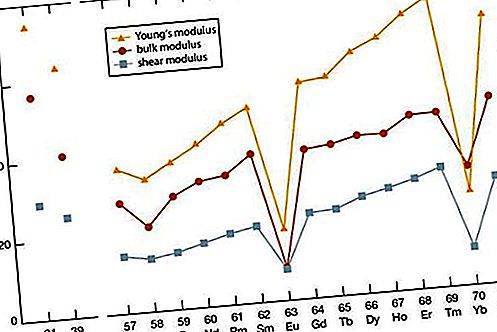
機械的性質
希土類金属は、弱い金属元素でも特に強い金属元素でもありません。また、適度な延性を示します。機械的特性は金属の純度と熱履歴に強く依存するため、文献で報告された値を比較することは困難です。極限強度は約120〜約160 MPa(メガパスカル)であり、延性は約15〜35%です。イッテルビウム(ユーロピウムは測定されていません)の強度は58 MPaとはるかに小さく、延性は2価金属で予想されるように約45%高くなっています。
化学的特性
希土類金属と空気との反応性は、軽いランタニドと重いランタニドの間に大きな違いを示します。軽いランタニドは、重いランタニド(ガドリニウムからルテチウムまで)、スカンジウム、およびイットリウムよりもはるかに速く酸化します。この違いの一部は、形成された酸化物生成物の変動によるものです。軽いランタニド(ランタンからネオジムまで)は、六角形のAタイプのR 2 O 3構造を形成します。中間のランタニド(サマリウムからガドリニウム)は、単斜B型のR 2 O 3相を形成します。一方、重いランタニド、スカンジウム、およびイットリウムは、立方CタイプのR 2 O 3修飾を形成します。Aタイプは、空気中の水蒸気と反応してオキシ水酸化物を形成します。これにより、白いコーティングが剥がれ、新しい金属表面が露出することで酸化が進行します。Cタイプの酸化物は、アルミニウムの挙動と同様に、それ以上の酸化を防ぐ堅固で密着したコーティングを形成します。BタイプのR 2 O 3相を形成するサマリウムとガドリニウムは、重いランタニド、スカンジウム、イットリウムよりもわずかに速く酸化しますが、それ以上の酸化を停止する密着コーティングを形成します。このため、軽いランタニドは真空または不活性ガス雰囲気で保管する必要がありますが、重いランタニド、スカンジウム、およびイットリウムは何も酸化せずに何年も屋外に放置することができます。
ユーロピウム金属はbcc構造を持ち、希土類の中で最も急速に湿った空気で酸化するため、常に不活性ガス雰囲気で処理する必要があります。ユーロピウムの湿った空気にさらされたときの反応生成物は、水和水酸化物、Eu(OH)2 ―H 2 Oです。これは、他のすべての希土類金属が酸化物を形成するため、異常な反応生成物です。
金属はフッ化水素酸(HF)を除くすべての酸と激しく反応し、H 2ガスを放出して対応する希土類アニオン化合物を形成します。希土類金属をフッ化水素酸に入れると、それ以上の反応を防ぐ不溶性のRF 3コーティングが形成されます。
希土類金属は、水素ガスと容易に反応してRH 2を形成し、強い水素化条件下では、三水素化物を形成しないスカンジウムを除いて、RH 3相になります。
化合物
希土類元素は数万の化合物を形成し、周期表の第7族金属(マンガン、テクネチウム、レニウム)の右側にあるすべての元素に加えて、遠くにあるベリリウムとマグネシウムも含まれますグループ2の左側。重要な化合物シリーズと、固有の特性または異常な動作をするいくつかの個々の化合物を以下に説明します。
酸化物
これまでに研究された無機希土類化合物の最大のファミリーは酸化物です。最も一般的な化学量論はR 2 O 3組成ですが、いくつかのランタニド元素には3+に加えて他の原子価状態があるため、他の化学量論が存在します。たとえば、酸化セリウム(CeO 2)、酸化プラセオジム(Pr 6 O 11)、酸化テルビウム(Tb 4 O 7)、酸化ユーロピウム(EuO)、Eu 3 O 4。ほとんどの議論は二元酸化物に集中しますが、三元および他の高次の酸化物も簡単に見直されます。