クラウジウス-クラペイロン方程式
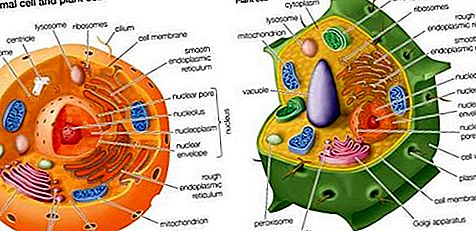
液体の水から蒸気への変換などの相変化は、一定温度での体積に伴う内部エネルギーの大きな変化があるシステムの重要な例です。図に示すように、シリンダーに圧力Pで水と蒸気の両方が平衡状態にあり、シリンダーが一定の温度Tに保持されているとします。両方の相が存在している限り、ピストンが上昇しても圧力は蒸気圧P vapに等しくなります。起こるすべてのことは、より多くの水が蒸気に変わり、熱リザーバーが温度を一定に保つために、蒸発潜熱λ= 1モルあたり40.65キロジュールを供給しなければならないということです。
前のセクションの結果を適用して、圧力による水の沸点の変化を見つけることができます。ピストンが上昇すると、1モルの水が蒸気に変わると仮定します。シリンダー内の体積の変化はΔV= V ガス − V 液体であり、V ガス = 30.143リットルは100°Cで1モルの蒸気の体積であり、V 液体 = 0.0188リットルは1モルの水の体積です。 。熱力学の第1法則により、定数PおよびTにおける有限プロセスの内部エネルギーの変化ΔUは、ΔU=λ−PΔVです。
したがって、水と蒸気の完全なシステムの一定Tでの体積によるUの変化は、
(48)
式(46)と比較すると、式(49)が得られます。ただし、現在の問題では、Pは蒸気圧Pvaporであり、Tのみに依存し、Vには依存しません。偏微分は、全微分と同じです。 (50)クラウジウス-クラペイロン方程式を与える
(51)
この方程式は、水と蒸気が平衡する圧力の温度、つまり沸騰温度の変化を与えるため、非常に役立ちます。V ガスと比較してV 液体を無視し、理想的なガスの法則から(52)を使用することにより、おおよその、しかしさらに有用なバージョンを取得できます。結果として得られる微分方程式は、次のように統合できます。
(53)
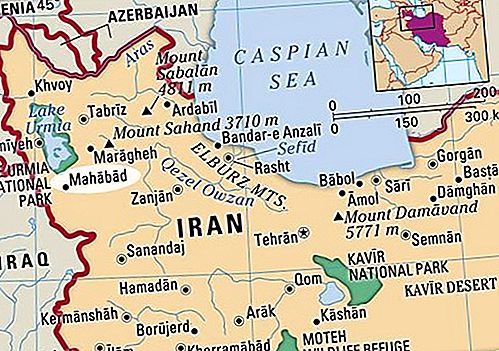
たとえば、エベレストの山頂では、気圧は海面での値の約30%です。R = 8.3145ジュール/ Kおよびλ= 40.65キロジュール/モルの値を使用すると、上記の式は水の沸騰温度に対してT = 342 K(69°C)であり、お茶を作るにはほとんど十分ではありません。