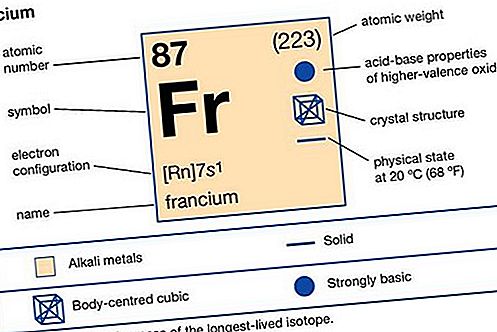
リン(P)、窒素族の非金属化学元素(周期表のグループ15 [Va])。室温では、暗闇で光る無色の半透明の柔らかなワックス状の固体です。
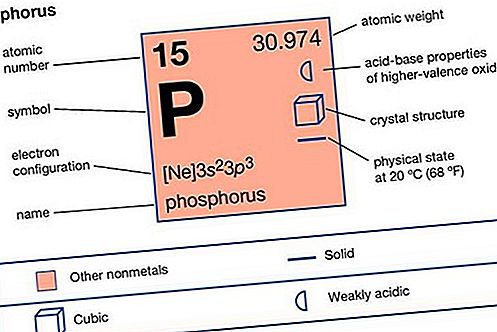
要素のプロパティ
| 原子番号 | 15 |
|---|---|
| 原子量 | 30.9738 |
| 融点(白) | 44.1°C(111.4°F) |
| 沸点(白) | 280°C(536°F) |
| 密度(白) | 20°C(68°F)で1.82グラム/ cm 3 |
| 酸化状態 | −3、+ 3、+ 5 |
| 電子配置 | 1s 2 2s 2 2p 6 3s 2 3p 3 |
歴史

12世紀のアラビアの錬金術師は偶然にリン元素を分離した可能性がありますが、その記録は不明です。リンは1669年に、錬金術を趣味としたドイツの商人、ヘニッヒブランドによって発見されたようです。ブランドでは、50バケットの尿を、彼らが化膿し「ワームを飼育」するまで放置しました。それから彼は尿をペースト状に煮詰め、砂でそれを加熱し、それにより混合物から元素リンを蒸留した。ブランドは彼の発見をゴットフリートウィルヘルムライプニッツへの手紙で報告し、その後、この要素の実証と暗闇で光るその能力、つまり「燐光」が公衆の関心を刺激しました。リンは、しかし、それが骨の成分であることが判明した約1世紀後まで、化学的好奇心のままでした。硝酸または硫酸で骨を消化するとリン酸が形成され、リンは木炭と一緒に加熱することで蒸留できます。1800年代後半、エジンバラのジェームズバージェスリードマンは、リン酸塩岩から元素を製造するための電気炉法を開発しました。これは、基本的に今日採用されている方法です。
発生と分布
リンは非常に広く分布している元素であり、crustEarthで12番目に豊富で、それには約0.10重量パーセント含まれています。その宇宙存在量は、標準のシリコン100原子あたり約1原子です。その高い化学反応性により、遊離状態では発生しません(いくつかの隕石を除く)。リンは常にリン酸イオンとして発生します。自然界の主要な複合形態はリン酸塩です。約550種類のミネラルにリンが含まれていることがわかっていますが、リンの主な供給源はアパタイトシリーズで、次の式に従って、リン酸イオンとさまざまな量のフッ化物、塩化物、または水酸化物イオンとともにカルシウムイオンが存在します[Ca 10(PO 4)6(F、Cl、またはOH)2]。その他の重要なリン含有ミネラルは、ウェーブライトとビビアナイトです。一般に、マグネシウム、マンガン、ストロンチウム、鉛などの金属原子は、鉱物中のカルシウムの代わりになり、ケイ酸塩、硫酸塩、バナジウム酸塩、および同様のアニオンは、リン酸塩イオンの代わりになります。フルオロアパタイトの非常に大きな堆積物は、地球の多くの場所で見られます。骨と歯のエナメル質のリン酸塩はヒドロキシアパタイトです。(フッ化物処理による虫歯の減少の原理は、ヒドロキシアパタイトの、より硬く、虫歯に強いフルオロアパタイトへの変換に依存します。)
主な商業的供給源は、炭酸塩を含むアパタイトの不純な塊状の形態である、亜リン酸塩、またはリン酸塩岩です。地球の地殻中の総リン酸塩岩の推定値は、平均約65,000,000,000トンで、そのうちモロッコと西サハラには約80%が含まれています。この推定値には、現在の方法で有用な製品に変換できるリン酸塩が十分に豊富な鉱石のみが含まれます。リン含有量の少ない大量の材料も存在します。

リンの天然に存在する唯一の同位体は、質量31のものです。質量24から質量46までの他の同位体は、適切な核反応によって合成されています。これらはすべて放射性であり、半減期は比較的短いです。質量32の同位体の半減期は14.268日であり、生体内のリンの吸収と移動を含むトレーサー研究で非常に有用であることが証明されています。

![メアリーアンダーソンアメリカの女優[1859-1940] メアリーアンダーソンアメリカの女優[1859-1940]](https://images.thetopknowledge.com/img/entertainment-pop-culture/9/mary-anderson-american-actress-1859-1940.jpg)