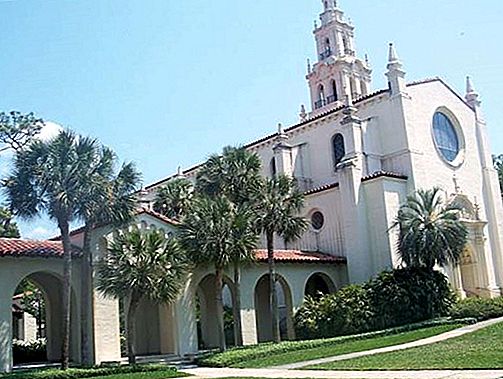
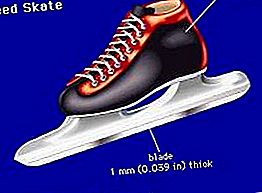
マグネシウム処理、様々な製品で使用するためのマグネシウム鉱石の準備。

マグネシウム(Mg)は銀色のホワイトメタルで、外観はアルミニウムに似ていますが、重量は3分の1です。1立方センチメートルあたりわずか1.738グラムの密度で、それは知られている最も軽い構造用金属です。六角形の最密充填(hcp)結晶構造を持っているため、この構造のほとんどの金属と同様に、低温で加工すると延性に欠けます。さらに、純粋な形では、ほとんどの構造用途に十分な強度がありません。しかしながら、合金化元素の添加は、特に軽量および高強度が重要である場合、鋳造および鍛造マグネシウム合金の両方が広く使用される程度までその特性を改善します。
マグネシウムは高温で酸素と強く反応します。乾燥した空気中で645°C(1,190°F)を超えると、明るい白色光と強い熱で燃焼します。このため、火薬にはマグネシウム粉末が使用されています。室温では、水不溶性の水酸化マグネシウムの安定した膜が金属の表面に形成され、ほとんどの雰囲気で腐食から保護されます。マグネシウムは、塩素、酸素、硫黄と安定した化合物を形成する強力な反応物質であるため、四塩化チタンからのチタンの製造や高炉鉄の脱硫など、いくつかの冶金学的用途があります。その化学的反応性は、産業、医学、および農業で幅広い用途を持つマグネシウム化合物でも明らかです。
歴史
マグネシウムの名前は、炭酸マグネシウム鉱物であるマグネサイトに由来し、この鉱物は、テッサリアの古代ギリシャの地域にあるマグネシアで発見されたマグネサイト鉱床に由来すると言われています。イギリスの化学者であるハンフリーデービーは、湿った硫酸マグネシウムを水銀として陰極として電解することにより、1808年にマグネシウムのアマルガムを生成したと言われています。しかし、最初の金属マグネシウムは1828年にフランスの科学者A.-A.-Bによって製造されました。忙しい。彼の研究は、金属カリウムによる溶融塩化マグネシウムの還元を含みました。1833年、イギリスの科学者マイケルファラデーは、溶融塩化マグネシウムの電気分解によってマグネシウムを最初に製造しました。彼の実験はドイツの化学者ロバート・ブンゼンによって繰り返されました。
最初の工業生産の成功は、溶融したカーナライトの電気分解に基づいて、1886年にアルミニウムとマグネシウムファブリクヘメリンゲンによってドイツで始まりました。ヘメリンゲンは後に1920年代から30年代にかけて工業用複合施設IG Farbenindustrieの一部となり、技術と同様に、1920年代と30年代に大量の溶融した、本質的に水を含まない塩化マグネシウム(現在はIG Farbenプロセスとして知られている)を製造するプロセスを開発しました。この製品を金属マグネシウムと塩素に電気分解するため。IGファルベンによる他の貢献は、数多くの鋳造および可鍛性合金の開発、精製および保護用フラックス、鍛造マグネシウム製品、および多数の航空機および自動車用途でした。第二次世界大戦中、米国のダウケミカルカンパニーと英国のマグネシウムエレクトロンリミテッドは、テキサス州ガルベストンベイとイギリスのハートルプールの北海から汲み上げられた海水から、マグネシウムの電解還元を始めました。同時にカナダのオンタリオで、LMピジオンの外部燃焼レトルト内で酸化マグネシウムをシリコンで熱還元するプロセスが導入されました。
戦争後、軍事申請は目立たなくなった。ダウケミカルは、鍛造製品、写真製版技術、表面処理システムを開発することにより、民間市場を拡大しました。抽出は、電解と熱還元に基づいて残りました。これらのプロセスには、レトルトの内部加熱(1961年にフランスで導入されたMagnethermプロセス)、脱水塩化マグネシウムプリルからの抽出(1974年にノルウェーの会社Norsk Hydroによって導入された)、および1970年頃。
2019年の時点で、中国は世界のマグネシウムの約85%を生産し、ロシア、カザフスタン、イスラエル、ブラジルは残りの大半を生産しています。
鉱石と原料
自然界で8番目に豊富な元素であるマグネシウムは、地球の地殻の2.4%を占めています。その強い反応性のために、それは自然の状態では発生しませんが、海水、塩水、および岩石のさまざまな化合物に含まれています。
鉱石鉱物の中で最も一般的なものは、炭酸塩ドロマイト(炭酸マグネシウムとカルシウムの化合物、MgCO 3・CaCO 3)とマグネサイト(炭酸マグネシウム、MgCO 3)です。あまり一般的ではないのは、水酸化物ミネラルブルーサイト、Mg(OH)2、およびハロゲン化物ミネラルカーナライト(塩化マグネシウムとカリウムの化合物と水、MgCl 2・KCl・6H 2 O)です。
塩化マグネシウムは、グレートソルトレイク(通常1.1重量パーセントのマグネシウムを含む)や死海(3.4パーセント)などの天然のブラインから回収できますが、最大の発生源は世界の海です。海水はわずか約0.13パーセントのマグネシウムですが、ほとんど無尽蔵の水源です。
採掘と集中
ドロマイトとマグネサイトの両方は、従来の方法で採鉱および濃縮されます。カーナライトは鉱石として掘られるか、溶液採掘によって表面に運ばれる他の塩化合物から分離されます。自然に発生するマグネシウム含有塩水は、太陽蒸発によって大きな池に集中します。
抽出と精製
強力な化学試薬であるマグネシウムは、安定した化合物を形成し、液体状態と気体状態の両方で酸素と塩素と反応します。これは、原材料からの金属の抽出が、十分に調整された技術を必要とするエネルギー集約型のプロセスであることを意味します。商業生産は、2つの完全に異なる方法に従います。塩化マグネシウムの電気分解またはピジョンプロセスによる酸化マグネシウムの熱還元です。電気分解はかつて世界のマグネシウム生産の約75パーセントを占めていました。しかし21世紀初頭、中国が世界の主要なマグネシウム生産国として台頭したとき、労働力とエネルギーのコストが低いため、ピジョンプロセスは電気分解ほど効率的ではありませんが、経済的に実行可能でした。
電解
電解プロセスは2つのステップで構成されます。塩化マグネシウムを含む原料の準備と、電解槽でのこの化合物の金属マグネシウムと塩素ガスへの解離です。
工業プロセスでは、細胞飼料は、無水の(本質的に水を含まない)塩化マグネシウム、部分的に脱水された塩化マグネシウム、または無水カーナライトを含むさまざまな溶融塩で構成されます。カーナライト鉱石に存在する不純物を回避するために、脱水された人工カーナライトは、加熱されたマグネシウムおよびカリウム含有溶液からの制御された結晶化によって生成されます。部分的に脱水された塩化マグネシウムは、海水をフロキュレーター内で軽く燃焼した反応性ドロマイトと混合するダウプロセスによって得ることができます。不溶性の水酸化マグネシウムが沈殿タンクの底に沈殿し、スラリーとしてポンプで送られ、ろ過され、塩酸との反応によって塩化マグネシウムに変換され、一連の蒸発ステップで水分が25%になるまで乾燥されます。最終脱水は製錬中に行われます。
無水塩化マグネシウムは、塩化マグネシウム塩水の脱水または酸化マグネシウムの塩素化という2つの主要な方法で製造されます。IGファルベンプロセスで例示される後者の方法では、軽く燃焼したドロマイトをフロキュレーターで海水と混合し、水酸化マグネシウムを沈殿させ、ろ過し、か焼して酸化マグネシウムにします。これを木炭と混合し、塩化マグネシウム溶液を加えて小球にして乾燥させる。小球は、レンガの裏打ちされたシャフト炉である塩素処理装置に装入され、そこで炭素電極によって約1,000〜1,200°C(1,800〜2,200°F)に加熱されます。炉のポートホールから導入された塩素ガスは、酸化マグネシウムと反応して溶融塩化マグネシウムを生成します。溶融塩化マグネシウムは、時々タップされて電解槽に送られます。
マグネシウムブラインの脱水は段階的に行われます。Norsk Hydroプロセスでは、沈殿物とろ過によって不純物が最初に除去されます。約8.5%のマグネシウムを含む精製ブラインは、蒸発により14%に濃縮され、プリリングタワーで微粒子に変換されます。この製品は、さらに水分を含まない粒子に乾燥され、電解槽に運ばれます。
電解セルは、基本的に、複数の鋼のカソードとグラファイトのアノードを備えたレンガで裏打ちされた容器です。これらは、セルフードを通して垂直に取り付けられ、アルカリ塩化物で構成される溶融塩電解液に部分的に沈められ、上記のプロセスで生成された塩化マグネシウムが6〜18%の濃度で添加されます。基本的な反応は次のとおりです。
動作温度は、680〜750°C(1,260〜1,380°F)です。消費電力は、生成されるマグネシウム1キログラムあたり12〜18キロワット時です。塩素とその他のガスがグラファイトのアノードで発生し、溶融マグネシウム金属が塩浴の上部に浮かび、そこで回収されます。塩素は脱水工程で再利用できます。
熱還元
熱生産では、ドロマイトはか焼されて酸化マグネシウム(MgO)と石灰(CaO)になり、これらはシリコン(Si)によって還元されて、マグネシウムガスとケイ酸二カルシウムのスラグが生成されます。基本的な反応は、
吸熱性です。つまり、熱を加えて持続させる必要があります。マグネシウムが1,800°C(3,270°F)で100キロパスカル(1気圧)の蒸気圧に達すると、熱要件は非常に高くなる可能性があります。反応温度を下げるために、工業プロセスは真空下で動作します。主な方法は3つあり、熱の供給方法が異なります。ピジョンプロセスでは、粉砕され、焼成されたドロマイトが、細かく粉砕されたフェロシリコンと混合され、ブリケット化され、円筒形のニッケルクロム鋼のレトルトに投入されます。いくつかのレトルトは、石油またはガス焚きの炉に水平に設置され、蓋と付属のコンデンサーシステムが炉から伸びています。1,200°C(2,200°F)の温度で13パスカルの減圧下で反応サイクルを行った後、マグネシウム結晶(クラウンと呼ばれる)が凝縮器から取り除かれ、スラグが固体として排出され、レトルトが再充填されます。ボルツァーノプロセスでは、ドロマイトフェロシリコンブリケットは、内部の電気加熱がチャージに伝達される特殊なチャージサポートシステムに積み重ねられます。完全な反応には、1,200°Cで400パスカル未満で20〜24時間かかります。
上記のプロセスで生成されたケイ酸二カルシウムスラグは、融点が約2,000°C(3,600°F)であるため、固体として存在しますが、装入物にアルミナ(酸化アルミニウム、Al 2 O 3)を追加すると、融点を1,550〜1,600°C(2,825〜2,900°F)に下げることができます。Magnethermプロセスで利用されるこの手法には、水冷銅電極を流れる電流によって液体スラグを直接加熱できるという利点があります。還元反応は、1,600°Cおよび400〜670パスカルの圧力で発生します。蒸発したマグネシウムは、反応器に接続された別のシステムで凝縮され、溶融スラグとフェロシリコンは間隔をあけて取り出されます。